POSSIBILE IPOTESI DEL MODELLO PARTICELLARE
(Conclusioni alle quali è giunta la classe, dopo il confronto e la discussione collettiva)
LE PARTICELLE:
1. SONO SUBMICROSCOPICHE( termine coniato dai ragazzi)
2. SONO LEGATE: i legami sono forti nello stato solido, sono meno forti nello stato liquido, quasi inesistenti negli aeriformi.
3. SI MUOVONO: la velocità è minima nei solidi (vibrazione su posizioni fisse); aumenta nei liquidi; aumenta ancora negli aeriformi.
4. LA VELOCITÁ DELLE PARTICELLE È IN RELAZIONE ALLA LORO ENERGIA TERMICA
5. HANNO TUTTE LE STESSE DIMENSIONI( almeno per quanto riguarda la stessa sostanza).
6. NON SONO CONTINUE NELLA LORO DISTRIBUZIONE
7. CIRCA LA LORO FORMA, NON RIUSCIAMO A GIUNGERE AD UNA CONCLUSIONE CONDIVISA, MA UNA BUONA PARTE DI NOI LE IMMAGINA DI FORMA PRESSOCHE’ SFERICA.
Abbiamo discusso molto per arrivare a queste conclusioni e la prof. ci ha aiutato a fare ordine nei ragionamenti.
PERCHE' SIAMO GIUNTI A QUESTE CONCLUSIONI?
• Il primo punto è evidente: se non riusciamo ad osservarle con i microscopi a disposizione, le particelle devono essere veramente molto piccole.
• Per il secondo punto, abbiamo riflettuto sugli stati della materia e le conclusioni ci sono sembrate le più plausibili con quanto si osserva sul loro comportamento.
• Anche per il terzo punto, ci siamo riferiti al comportamento della materia nei tre stati. Infatti, se pensiamo ad un odore, questo si avverte anche molto lontano dalla fonte.
• Deve per forza esserci una relazione fra la loro velocità e il calore fornito, basta pensare ai passaggi di stato dell’acqua, che abbiamo già studiato.
• Abbiamo pensato che, almeno per uno stesso tipo di sostanza, le particelle dovrebbero avere le stesse dimensioni altrimenti cambierebbe la sostanza. Naturalmente potrebbe essere diversamente, ma siamo orientati a pensare in questo modo, non avendo prove.
• Questo lo abbiamo ipotizzato riferendoci alla diffusione di un liquido colorato nell’acqua o alla dissoluzione del sale e dello zucchero nell’acqua, tutti fenomeni che abbiamo già studiato.
• Questo punto ci ha fatto discutere molto e non siamo giunti ad una ipotesi condivisa. Un compagno sostiene che le particelle devono avere una forma sferica o similare perché con questa forma la materia si distribuisce in maniera omogenea e poi così occupa meno spazio. Una buona parte di noi ha accettato la sua ipotesi ma altri sono scettici, anche se non hanno saputo offrire un’ipotesi alternativa.
Adesso disponiamo di un'ipotesi condivisa alla quale ci riferiremo, come a un possibile modello della struttura particellare della materia.
Proveremo a vedere se e come funziona negli esperimenti, che faremo, o se, invece, dovremo apportare delle correzioni a tale modello.
*****
Nei prossimi post,saranno illustrati alcuni esperimenti, che sono stati interpretati dai ragazzi alla luce dell'ipotesi particellare, da essi formulata.
Attraverso tali esperimenti si è cercato di trovare conferma circa "la bontà" di tale ipotesi, confrontando il modello particellare con i dati sperimentali ottenuti e valutandone la coerenza con quello.
I problemi affrontati sono:
1. Osservare l'ebollizione dell'acqua e interpretare il fenomeno alla luce dell'ipotesi particellare.
2. A parità di altre condizioni( quantità di calore fornito, tempo di esposizione al calore), la quantità di acqua evaporata dipende dalla superficie di evaporazione?
3. A parità di altre condizioni( due becker uguali, volume iniziale d'acqua, tempo di esposizione alla fiamma) la quantità di acqua evaporata dipende dal calore fornito?
S i riporta qui il primo di tali esperimenti: L'EBOLLIZIONE DELL'ACQUA
MATERIALE
• 1 fornelletto a gas
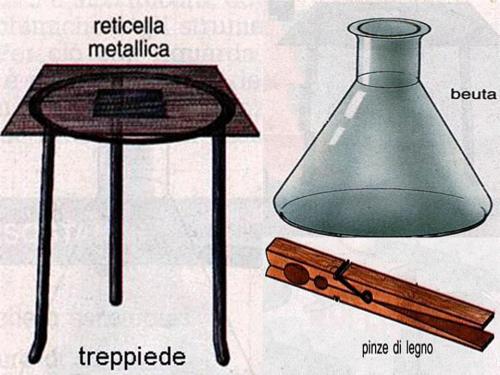
• 1 treppiedi metallico
• 1 reticella frangifiamma
• 1 termometro a mercurio
• 1 molletta di legno
• 1 piastrella x supporto al fornello
• 1 beuta
• 250 ml di acqua
PROCEDIMENTO
- Abbiamo sistemato il fornelletto a gas sulla piastrella di ceramica per isolarlo dal fondo del tavolo da lavoro.
- Abbiamo posizionato il treppiede in modo che sormontasse il fornelletto.
- Abbiamo posto sul treppiede la reticella frangifiamma.
- Abbiamo sistemato la beuta sopra la reticella.
- Abbiamo acceso il fornello.
- Con il termometro, abbiamo misurato la temperatura iniziale e quindi abbiamo proseguito con il rilevamento ogni due minuti fino a raggiungere la temperatura di ebollizione dell’acqua, compilando la seguente tabella e realizzando il grafico relativo.
- Alle 12.08 abbiamo effettuato l’ultimo rilevamento e poi spento il fornelletto.
TABELLA

GRAFICO

OSSERVAZIONI
- La temperatura sale progressivamente al passare del tempo man mano che si fornisce calore.
- A 65°C circa, notiamo che il livello dell’acqua nella beuta è superiore a 250 ml nonostante l’evaporazione ‘porti via’ un certo quantitativo di sostanza.
- A 75°C , il vetro si appanna e scendono delle goccioline dal bordo lungo le pareti della beuta.
- A 90°C , il livello dell’acqua è ancora superiore a 250 ml nonostante la massiccia evaporazione.
- A 100°C l’acqua bolle e si osservano movimenti tumultuosi dell’intera massa, la superficie è interessata da una evaporazione al ‘top’.
- Per altri quattro rilevamenti, osserviamo che la temperatura rimane ferma a 100 °C; nonostante si continui a fornire calore alla beuta, c’è come una sosta nella temperatura(sappiamo già, perché lo abbiamo sperimentato, che la temperatura rimane con un pianerottolo a 100°C finchè l’acqua non è evaporata del tutto).
- Abbiamo rilevato il livello dell’acqua, a pomeriggio, quando tutto il sistema si era raffreddato a circa 21°C, ed abbiamo osservato che era sceso a circa 210 ml.
• Il fatto che, fra 65 °C e 90°C, il volume dell’acqua sia aumentato ci sembra in accordo con l’ipotesi particellare: infatti il calore assorbito dall’acqua serve a fare diventare più veloci le sue particelle, che, acquistando energia, allentano i propri legami distanziandosi e quindi il volume complessivo aumenta.
• Il fatto che la temperatura rimanga a 100°C fino a quando l’acqua bolle e non si è trasformata completamente in vapore acqueo, si spiega con il fatto che il calore fornito serve alle particelle per rompere i legami e per passare allo stato aeriforme; anche questo sembra in accordo con l’ipotesi particellare.
• Anche il diminuito volume dell’acqua, a raffreddamento avvenuto, interrotta l’ebollizione, conferma che circa 40 ml di acqua si sono trasformati in vapore acqueo abbandonando lo stato solido, grazie al calore fornito.
DOMANDE RIMASTE APERTE:
1. Perché a 90°C, il volume dell’acqua è superiore a quello iniziale nonostante la massiccia evaporazione in atto?
2. La dilatazione del liquido è sufficiente a spiegare l’aumento di volume?
Il modello particellare dovrebbe permetterci di fare delle previsioni in merito. La prof. dice che cercheremo di dare delle risposte il prossimo anno riprendendo la sperimentazione.
Per la fine dell’anno porteremo avanti il percorso ipotizzato per non rischiare di disperderci.
Per oggi si conclude qui! Il seguito al prossimo post.
bene, bene! Hai ripreso con la pubblicazione di temperatura & calore. Pensavo che avessi smesso!
RispondiElimina